Untuk membuat sediaan obat cair, pertama-tama perlu diketahui parameter-parameter penting dari zat aktif itu sendiri seperti : kelarutan, pH stabil (bukan pH pada saat dilarutkan dalam air, tetapi pH medium yang membuat senyawa itu stabil), rute degradasi utama, sifat asam basa, nilai pKa dan inkompatibilitas.
Seperti contoh dibawah ini, dilakukan studi preformulasi sederhana terhadap aspirin.
Berdasarkan data-data yang diperoleh dari studi pre-formulasi sederhana ini, setidaknya ada beberapa masalah yang dihadapi ketika seorang formulator ingin membuat sebuah sediaan cair aspirin. Pertama adalah masalah kelarutan dan stabilitas. Aspirin adalah senyawa asam yang kurang larut dalam air (1:300). Sebenarnya, dengan menggunakan prinsip Handerson-Hasselbalch, kelarutan aspirin dalam air dapat ditingkatkan dengan cara membuat aspirin menjadi terionkan. Hal ini bisa ditempuh dengan mengubah pH medium menjadi lebih besar atau sama dengan $pk_a + 2$ yaitu $3,5 + 2 = 5,5$. Sayangnya, mengubah pH juga bukan merupakan solusi cerdas karena aspirin justru tidak stabil pada pH 4 - 8.
Berdasarkan data yang sangat terbatas ini, bagaimana usulan yang logis agar aspirin mampu diformulasikan menjadi sediaan cair yang berkualitas?
Daftar Pustaka
[1] S. C. Sweetman, Ed., Martindale The Complete Drug Reference, 6th ed. London, 2009.
[2] National Center for Biotechnology Information, “PubChem Database. Aspirin, CID=2244.” [Online]. Available: https://pubchem.ncbi.nlm.nih.gov/compound/Aspirin. [Accessed: 13-Oct-2019].
[3] S. Yoshioka and J. V. Stella, Stability of Drugs and Dosage Forms. New York: Kluwer Academic Publishers, 2002.
[4] Chemaxon, “Solubility Predictor,” 2018. [Online]. Available: https://disco.chemaxon.com/apps/demos/solubility/. [Accessed: 13-Oct-2019].
Seperti contoh dibawah ini, dilakukan studi preformulasi sederhana terhadap aspirin.
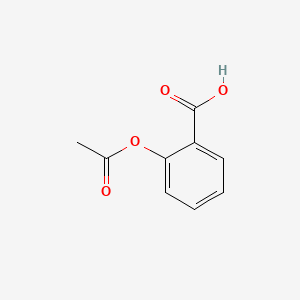 |
| Gambar 1. Struktur molekul aspirin [2] |
| No | Parameter | Deskripsi/data | Ref |
| 1 | Khasiat | Sebagai analgesik dan antipiretik dengan cara menghambat enzim sikooksigenase dalam proses pembentukan prostaglandin | [1] |
| 2 | Dosis terapi | Dosis lazim aspirin yang diberikan melalui rute oral sebagai analgesik dan antipiretik adalah 300 – 900 mg setiap 4 – 6 jam tergantung pada kebutuhan klinis, dengan dosis maksimal 4 g per hari. | [1] |
| 3 | Berat Molekul | 180,16 g/mol | [2] |
| 4 | Kelarutan | Larut 1 dalam 300 bagian air, 1 dalam 5 bagian alkohol, 1 dalam 17 bagian kloroform, 1 dalam 10 – 15 bagian eter | [1] |
| 5 | Titik lebur | 135°C | [2] |
| 6 | Titik didih | 140°C | [2] |
| 7 | Dekomposisi | Terdekomposisi pada suhu 140°C | |
| 8 | Pemerian | Kristal berwarna putih umumnya berbentuk tabung atau seperti jarum, atau serbuk kristalin putih. Tidak berbau atau mempunyai bau yang lemah. Stabil di dalam udara kering, pada udara lembab akan mengalami hidrolisis secara bertahap menjadi asam salisilat dan asam asetat | [1] |
| 9 | Reaksi degradasi utama | hidrolisis | [3] |
| 10 | log P | 1,19 | [2] |
| 11 | pKa (Gugus fungsi) | 3,5 pada suhu 25°C (asam karboksilat, COOH) | [2] |
| 13 | pH stabil | Dalam larutan berair, aspirin paling stabil pada pH 2 – 3, kurang stabil pada pH 4 – 8, paling tidak stabil pada pH kurang dari 2 atau lebih dari 8. Larutan aspirin jenuh dalam pelarut air pada pH 5 – 7 akan mengalami hidrolisis dengan sempurna sekitar 1 minggu | [2] |
| 14 | Inkompatibilitas | Tidak kompatibel dengan oksidator, asam kuat, basa kuat, dapat bereaksi dengan air atau nukleofil (gugus amina atau hidroksi), dapat bereaksi dengan asetanilida, amidopirin, fenazon, heksamin, garam besi, fenobarbiton sodium, garam kinin, kalium dan natrium iodida, alkali hidroksida, karbonat, stearat, dan paracetamol. | [2] |
Berdasarkan data-data yang diperoleh dari studi pre-formulasi sederhana ini, setidaknya ada beberapa masalah yang dihadapi ketika seorang formulator ingin membuat sebuah sediaan cair aspirin. Pertama adalah masalah kelarutan dan stabilitas. Aspirin adalah senyawa asam yang kurang larut dalam air (1:300). Sebenarnya, dengan menggunakan prinsip Handerson-Hasselbalch, kelarutan aspirin dalam air dapat ditingkatkan dengan cara membuat aspirin menjadi terionkan. Hal ini bisa ditempuh dengan mengubah pH medium menjadi lebih besar atau sama dengan $pk_a + 2$ yaitu $3,5 + 2 = 5,5$. Sayangnya, mengubah pH juga bukan merupakan solusi cerdas karena aspirin justru tidak stabil pada pH 4 - 8.
Berdasarkan data yang sangat terbatas ini, bagaimana usulan yang logis agar aspirin mampu diformulasikan menjadi sediaan cair yang berkualitas?
Daftar Pustaka
[1] S. C. Sweetman, Ed., Martindale The Complete Drug Reference, 6th ed. London, 2009.
[2] National Center for Biotechnology Information, “PubChem Database. Aspirin, CID=2244.” [Online]. Available: https://pubchem.ncbi.nlm.nih.gov/compound/Aspirin. [Accessed: 13-Oct-2019].
[3] S. Yoshioka and J. V. Stella, Stability of Drugs and Dosage Forms. New York: Kluwer Academic Publishers, 2002.
[4] Chemaxon, “Solubility Predictor,” 2018. [Online]. Available: https://disco.chemaxon.com/apps/demos/solubility/. [Accessed: 13-Oct-2019].
Komentar
Posting Komentar